UPDATE: die EU hat die MDR im Amtsblatt am 5. Mai 2017 veröffentlicht.
Das Thema Klassifizierung, vor allem Klassifizierung von Software, beschäftigt die Fachwelt seit die aktuelle Fassung der MDR auf der Webseite der Europäischen Kommission veröffentlicht wurde.
Auch Prof. Christian Johner hat in seinem Blog bereits einen Artikel zur Regel 11 verfasst und die Probleme erläutert.
Der Anhang VII der MDR beschreibt die Klassifizierungskriterien. Für Software gilt nach Kapitel II Punkt 3:
- Software als Teil eines Medizinprodukts, fällt automatisch in dieselbe Klasse wie das Gerät.
- Software, die von einem Medizingerät unabhängig ist, wird selbst klassifiziert.
Weiterhin gilt, dass Software als aktives Medizingerät zu betrachten ist. Allerdings gibt es mit der Regel 11 nun eine eigenständige Vorschrift, wie Software zu klassifizieren ist:
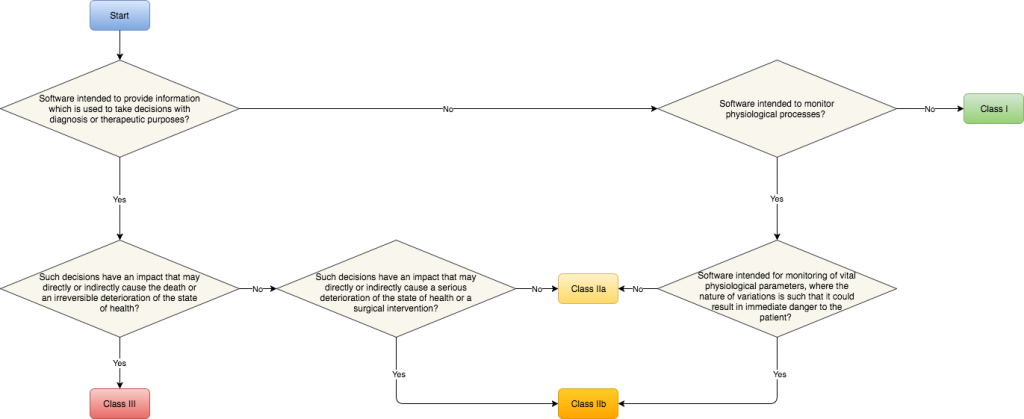
Anhand der Grafik ist gut erkennbar, dass es in Zukunft kaum noch Klasse I Software geben wird. Ist die Zweckbestimmung der Software, Informationen zur Diagnose oder zur Therapie zur Verfügung zu stellen, landet man mindestens in Klasse IIa. Die Anforderungen an das Verfahren der Konformitätserklärung ist für Klasse IIa im Vergleich zur Klasse I deutlich erweitert. Unter anderem wird ein zertifiziertes Qualitätsmanagementsystem gefordert und zur in-Verkehr-Bringung muss die benannte Stelle mit einbezogen werden.
MDR – Diskussion
Ich persönlich finde die Klassifizierungsregeln ein wenig unglücklich formuliert. Ein Beispiel:
„[…] may directly or indirectly cause the death […]“
Jeder, der schon einmal eine Risikoanalyse durchgeführt hat, weiß, dass es Medizinprodukte gibt, die möglicherweise direkt oder indirekt zum Tod führen können (Bsp.: Strahlentherapie). Was hier aber fehlt, ist die Wahrscheinlichkeit mit der dieser Fall eintritt.
Wenn ich mir beispielsweise eine App anschaue, die dazu dient, die notwendige Insulindosis zu berechnen, dann ist jedem bewusst, dass eine zu hohe oder zu niedrige Dosis zum Tod führen kann. Klar ist aber auch, dass dies in der Risikoanalyse berücksichtigt wird, und dass diese Risiken zu mitigieren sind. In diesem Fall, würde das vielleicht bedeuten, dass die Funktion, welche den Insulinwert berechnet, mit entsprechenden Prüfungen versehen ist, um falsche Werte zu vermeiden, und der Patient zusätzlich auch noch einen Warnhinweis findet, dass er bei großen Dosisabweichungen einen Arzt aufsuchen soll, bevor er das Medikament nimmt.
Gehen wir nun davon aus, dass der Hersteller alles Erdenkliche unternommen hat, um das Risiko zu minimieren. Fakt ist, dass eine Software nie fehlerfrei ist. Das heißt aber auch, dass die Software nach wie vor möglicherweise, vielleicht, eventuell direkt oder indirekt zum Tod führen könnte. Und schon habe ich eine Software Klasse III.
Ich habe den Eindruck, dass das Ziel hier ein wenig verfehlt wurde. Anders ausgedrückt: gibt es dann überhaupt noch Medizintechnik-Software Klasse I?
- Kommunikation – unser Jahresmotto 2020 - 17. Dezember 2020
- MDR verschoben und §120 Übergangsregelung VS Design Changes - 31. März 2020
- Männer, die auf Excel starren - 7. November 2019

